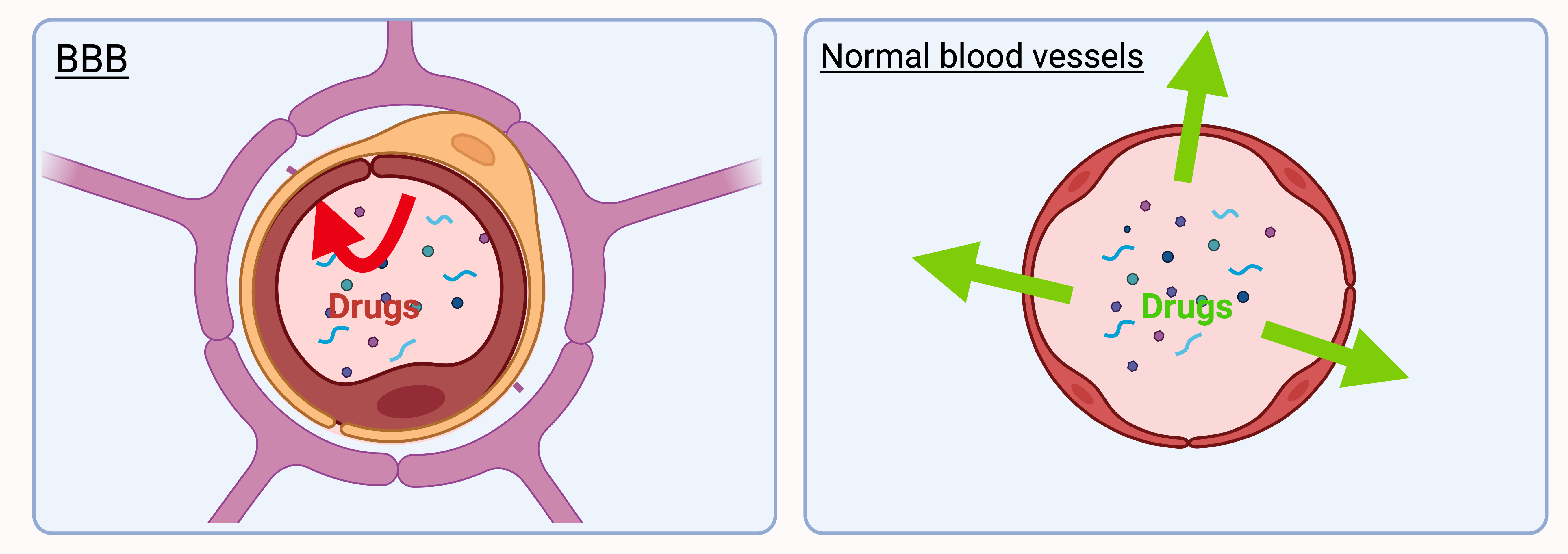
En effet, ce dernier est protégé par ce qu’on appelle la barrière hémato-encéphalique (ou BHE) qui, d’un côté, empêche que des molécules toxiques accèdent au cerveau mais, de l’autre, limite l’accumulation des médicaments à doses thérapeutiques dans ce même cerveau.
Cette BHE est en fait une barrière qui se situe autour des vaisseaux sanguins qui irriguent le cerveau et qui empêche les molécules étrangères circulant dans le sang de passer dans le système nerveux central.
Bien sûr, certaines molécules arrivent à traverser la BHE, notamment si elles sont de petite taille, plutôt solubles dans les graisses (« lipophiles ») et peu ionisées, mais le développement et le transfert aux patients d’une majorité de molécules à fort potentiel thérapeutique sont limités par leur faible pénétration de la BHE.
C’est pourquoi de nombreux chercheurs travaillent sur des stratégies permettant d’améliorer l’accès des médicaments au cerveau.
Quelles stratégies ?
Certaines de ces stratégies peuvent être invasives (injection directe dans le cerveau), mais elles sont peu adaptées à des maladies chroniques comme la SEP.
Une option plus acceptable est d’ouvrir de façon passagère la BHE, soit en utilisant une solution hypertonique, soit en utilisant des moyens physiques comme les ultrasons focalisés. Mais ces méthodes sont peu spécifiques, car elles ouvrent la BHE à toutes les molécules présentes dans le sang, y compris des molécules éventuellement toxiques.
Alternativement, les chercheurs ont développé des stratégies visant à employer les mécanismes naturels utilisés par l’organisme pour amener les éléments essentiels dont le cerveau a besoin, comme le glucose, les acides aminés ou l’insuline.
Ces éléments sont transférés du sang au cerveau via des transporteurs ou via des récepteurs spécifiques présents à la surface des vaisseaux sanguins de la BHE. Il est ainsi possible de modifier la molécule thérapeutique de telle façon que l’organisme la considère comme un de ces éléments et la transporte à travers la BHE. Ceci nécessite une modification chimique de la molécule, sans modifier son action thérapeutique, ce qui n’est pas toujours possible et ce qui doit être optimisé individuellement pour chaque molécule.
Une autre option est d’encapsuler la molécule d’intérêt dans un véhicule qu’on appelle nanomédecine. Ces nanomédecines sont des petites particules sphériques de taille nanométrique (entre 100 et 200 nm en général) et qui peuvent embarquer en leur sein toute une série de molécules. La surface de ces nanomédecines peut être ainsi modifiée pour qu’elles interagissent avec les récepteurs ou transporteurs présents dans les vaisseaux sanguins de la BHE. L’avantage est que les nanomédecines protègent les molécules thérapeutiques fragiles, les solubilisent, si elles ne sont pas solubles dans l’eau, et facilitent leur transport. En outre, par rapport à la modification directe de la molécule, on ne risque pas de l’inactiver en l’encapsulant dans une nanoparticule et, une fois la nanomédecine ou sa surface modifiée, ce véhicule est valable pour quasiment n’importe quelle molécule.
Enfin, une autre possibilité est de changer la voie d’administration de la molécule d’intérêt. La majorité des médicaments est administrée soit par voie orale soit par voie intraveineuse. Mais pour éviter que la molécule ne soit bloquée par la BHE, on peut utiliser alternativement une administration nasale ciblant la muqueuse olfactive : le Nose-to-Brain ou N2B.
Dans ce cas-ci, l’administration est non invasive et la molécule peut traverser la muqueuse olfactive et atteindre directement le cerveau.
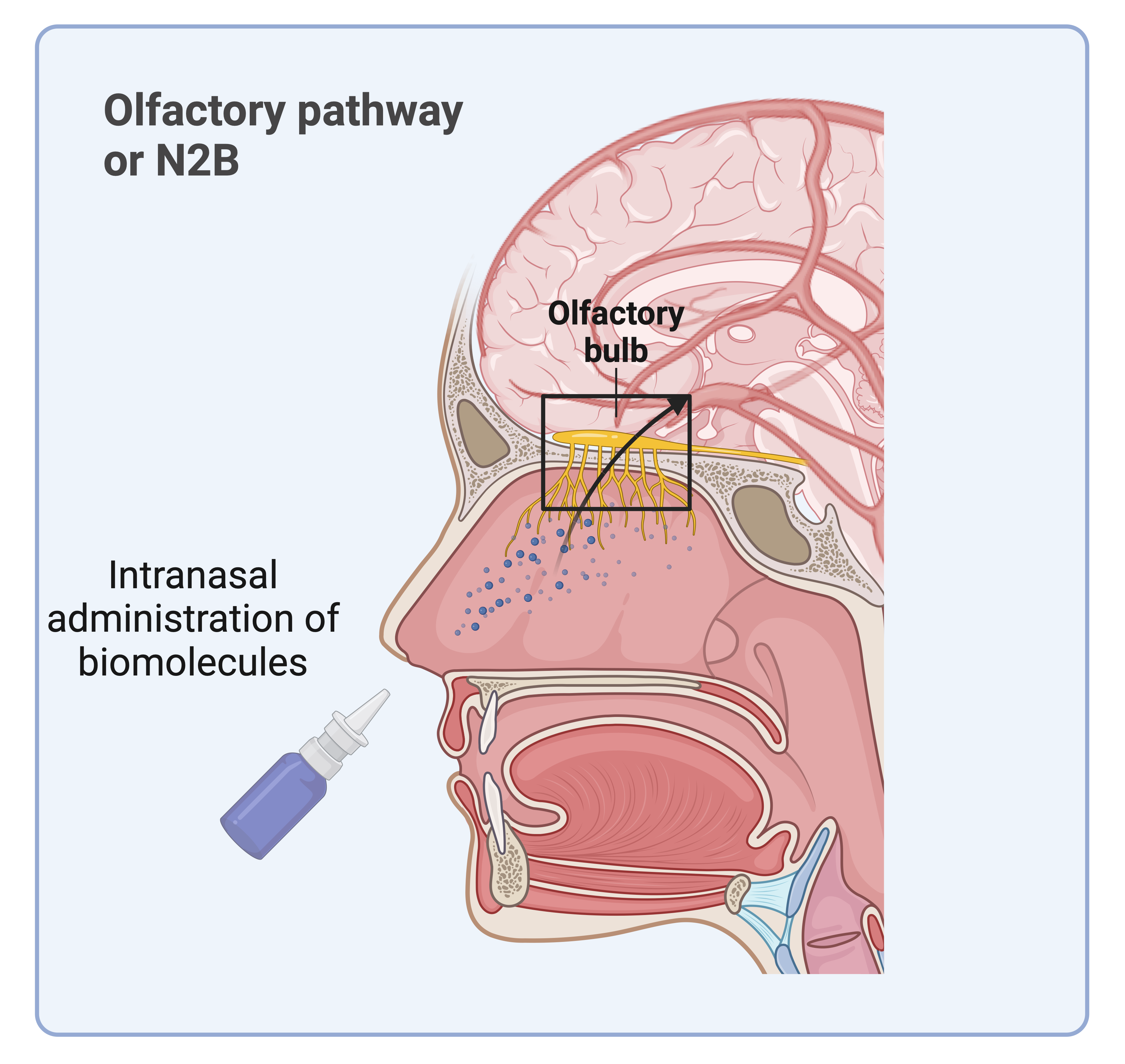
Bien sûr, il y a aussi des limitations, comme un passage du médicament au travers de la muqueuse nasale (ce qui l’amène dans la circulation sanguine). Mais de plus en plus de travaux visent à développer cette voie, soit en proposant des sprays nasaux qui permettent une administration préférentielle dans la zone olfactive (Optinose™), soit en jouant sur la façon dont le médicament est formulé, incluant des nanomédecines, pour qu’il passe plus facilement la barrière olfactive.
Prof. Anne des Rieux, Louvain Drug Researsh Institue, UCLouvain
